オファツムマブは、腫瘍細胞表面にあるCD20抗原というタンパク質に結合し、腫瘍細胞を破壊する作用を持つ新規のヒトモノクローナル抗体薬です。オファツムマブは、慢性リンパ性白血病(CLL)に対する治療薬として、2009年に米国で、2010年には欧州で承認されました。また、日本では再発又は難治性のCLLに対する治療薬として2013年3月に承認されました。CLL以外では、低悪性度のB細胞性非ホジキンリンパ腫(B-NHL)を対象として、2つの国際的な第3相臨床試験が行われています。
1. 再発の低悪性度B-NHLを対象とした臨床試験
2010年10月より、再発の濾胞性リンパ腫の患者さんを対象に、オファツムマブ単剤療法の効果と安全性を調べるため、国際的な第3相試験が開始されました。その後、2014年に試験の計画が変更され、現在、再発の低悪性度B-NHLを対象に試験が行われています。
臨床試験の名称:「リツキシマブ療法後の再発性濾胞性リンパ腫患者を対象としたオファツムマブ単剤療法とリツキシマブ単剤療法との比較試験」
この臨床試験の目的は、オファツムマブ単剤療法を受けた患者さんと、リツキシマブ単剤療法を受けた患者さんについて、効果と安全性を比較することです。対象となるのは、リツキシマブ療法を受けた後に再発したB-NHLの患者さんです。この臨床試験は、日本を含む世界各国の医療機関が共同して、現在(2014年12月時点)も行われています。国内では、以下の都道府県にある医療機関のいくつかで、この臨床試験が行われます。
宮城県、栃木県、埼玉県、東京都、愛知県、京都府、長崎県
2. 治療抵抗性の低悪性度B-NHLを対象とした臨床試験
2010年8月より、治療抵抗性の低悪性度B-NHLの患者さんを対象に、オファツムマブとベンダムスチンとの併用療法の効果と安全性を調べるため、国際的な第3相試験が開始されました。
臨床試験の名称:「リツキシマブ治療抵抗性B-NHL患者を対象としたオファツムマブおよびベンダムスチン併用療法とベンダムスチン単剤療法との比較試験」
この臨床試験の目的は、オファツムマブとベンダムスチンとの併用療法を受けた患者さんと、ベンダムスチン単剤療法を受けた患者さんについて、効果と安全性を比較することです。対象となるのは、リツキシマブ療法の効果が十分に得られなかった(治療抵抗性の)B-NHLの患者さんです。この臨床試験は、日本を含む世界各国の医療機関が共同して、現在(2014年12月時点)も行われています。国内では、以下の都道府県にある医療機関のいくつかで、この臨床試験が行われます。
宮城県、茨城県、東京都、神奈川県、愛知県、大阪府、兵庫県、岡山県、広島県、福岡県
これらの臨床試験に関するより詳しい情報(お問合せ先を含む)は、以下の医薬品情報データベースに公開されています。
>>医薬品情報データベース
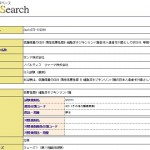
検索をする際には、「臨床試験情報」のボタンをクリックし、「疾患名」に「リンパ腫」、「試験薬剤名」に「オファツムマブ」と入力し、「検索」ボタンをクリックします。
臨床試験を実施しているグラクソ・スミスクライン株式会社では、臨床試験の適正な実施や患者さんの個人情報保護などの観点から、医療関係者以外の方からのお問合せには対応していませんので、ご了承ください。
なお、一般的に臨床試験は、従来の治療薬や治療法よりも有効であると期待される新薬や新しい治療法などについて、その有効性や安全性などを確かめることを目的として行われますが、期待された効果がみられない場合や、思わぬ副作用が生じる場合もあります。臨床試験への参加を考慮する際には、主治医の先生ともよく話し合い、十分に納得し同意した上で、参加することをお勧めいたします。
(※)上記の内容は、このページに掲載された時点での情報に基づいています。また、リンパ腫などに関する臨床試験の情報を提供することを目的としており、特定の臨床試験への参加を推奨することを目的とはしておりません。
(関連リンク)
>>臨床試験(治験)とは何かを知りたい方へ
(国立がん研究センターがん情報サービス)
>>臨床試験(治験)への参加を考えている方へ
(国立がん研究センターがん情報サービス)